انواع باتری موضوعی است که در این مقاله به آن می پردازیم و خواهیم دید که در پی ال سی برند دلتا که یکی از مهمترین تجهیزات اتوماسیون هستند نیز به کار می روند.برای شناخت باتری ها لازم است تعریفی از آنها داشته باشیم و سپس ضمن نگاه اجمالی به سرگذشت آنها، خصوصیات هریک را بررسی کنیم.
باتری چیست؟
باتری ها نوعی منبع تأمین بی وقفه انرژی به شمار می روند. این باتری ها با توجه به قابلیت شارژ و دشارژشان، کاربردهای زیادی در صنایع مختلف پیدا کرده اند.
به طور کلی باتری ها دارای اندازه های مختلف و قدرت های متفاوتی هستند که همین امر باعث میشود کارایی آن ها نیز متفاوت باشد. برخی از باتری ها برای کاربردهای صنعتی طراحی و تولید می شوند.این باتری ها که به باتری های صنعتی معروفند از توان بالاتری برخوردار بوده و قابلیت ذخیره انرژی الکتریسیته آنها بیشتر است. در واقع باتری ها منبع تأمین انرژی بی سیم برای انواع تجهیزات و ماشین آلات در تأسیسات صنعتی هستند. این موضوع در تأسیسات الکتریکی پررنگ تر است .

سرگذشت باتری، اهمیت و اساس کار آن
در واقع اختراع باتری زمانی آغاز شد که الساندرو ولتا فیزیکدان ایتالیایی توانست از مایعی خالص و رسانا به صورت پیوسته برق تولید نماید. این کشف سرآغاز تولید انواع باتری ها خصوصا باتری هایی الکتریکی شد. شاید ما این موضوع را ندانیم که باتری ها در زندگی روزمره ما نقش زیادی دارند. در واقع باتری ها منبع انرژی بسیار مهمی به شمار می روند. از موتورهای ماشین ها و ابزارهای پزشکی گرفته تا دستگاه های ارتباطی، گوشی های هوشمند، لپ تاپ ها، ساعت ها، و هر جایی که فکر کنید باتری ها کاربرد دارند. این سطح گسترده استفاده از باتری ها نشان دهنده ی اهمیت آنهاست. این اهمیت به قدری بوده است که که در سال 2019 جایزه نویل شیمی به سه دانشمند برای توسعه باتری های یون لیتیم اعطا شد.از این رو بررسی نحوه کارکرد و شناخت انواع آنها را می طلبد.
اساس کار باتری ها
باتری مجموعه ای از یک یا چند سلول است. سلول یک واحد الکتروشیمیایی است که ذخیره انرژی باتری را عهده دار است. هر سلول از سه جزء تشکیل شده است: دو الکترود و یک الکترولیت.
الکترودها، خود به دو نوع کاتد و آند تقسیم می شوند. تأمین انرژی باتری ها توسط فرآیندهای شیمیایی اکسایش – کاهش که در الکترولیت رخ می دهد، انجام می شود.
الکترود کاتد، همان قطب منفی باتری بوده و الکترود آند قطب مثبت باتری است. وقتی آند اکسید می شود الکترون از دست داده و این الکترون ها وارد مدار خارجی می شوند سپس، کاتد الکترون ها را از مدار داخلی می پذیرد.
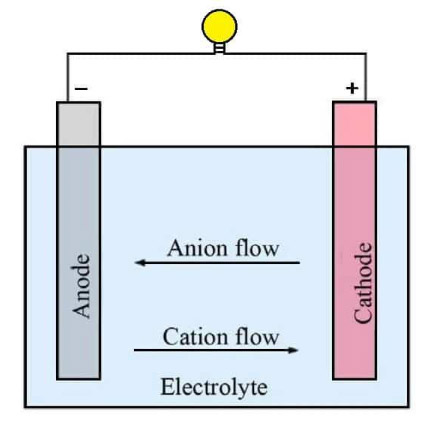
انواع باتری الکتریکی
باتری ها به دو دسته کلی باتری های اولیه (غیر قابل شارژ) و باتری های ثانویه (قابل شارژ) تقسیم می شوند:
باتری های اولیه
نسل اول باتری ها یا باتری های اولیه همان باتری های غیرقابل شارژ هستند که قادر به شارژ الکتریکی نیستند. این باتری ها فقط یک بار استفاده می شوند. باتری های غیر قابل شارژ، باتری های خشک نیز نام دارند. باتری های اولیه ارزان قیمت و سبک وزن بوده و نیاز به نگهداری خاصی ندارند. اکثر این نوع باتری ها، مانند باتری ها قلیایی، دارای شکل استوانه ای هستند.
از جمله باتری های اولیه می توان به باتری های خشک مورد استفاده در ریموت تلویزیون، ساعت ها و … اشاره نمود. در چنین سلول هایی یک محفظه حاوی روی به عنوان آند عمل کرده و یک میله کربنی به عنوان کاتد عمل می نماید. مخلوطی از منگنز دی اکسید و کربن در اطراف کاتد قرار می گیرد. فضای خالی بین آنها (محفظه و میله) با خمیری مرطوب از جنس آمونیوم کلراید و روی کلراید پر می شود.
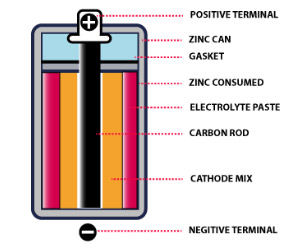
در این باتری ها واکنش های ریداکس (اکسایش و کاهش) تنها در یک جهت انجام می شوند. واکنش دهنده ها پس از مدتی تمام می شوند و همین موضوع باعث می شود فقط یک بار مورد استفاده قرار گیرند.
در سمت آند واکنش زیر رخ می دهد:
![]()
در سمت کاتد واکنش زیر رخ می دهد:
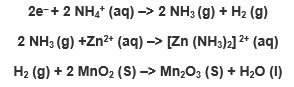
بنابراین، واکنش کلی به صورت زیر است:
![]()
مثال دیگر از سلول های اولیه سلول جیوه است، که در آن آمالگام روی-آمالگام به عنوان آند و کربن به عنوان کاتد استفاده می شود. خمیری از HgO نیز به عنوان الکترولیت فضای بین آنها را پر کرده است. این سلول ها تنها در دستگاه هایی استفاده می شوند که نیاز به تأمین جریان الکتریکی نسبتاً کمی دارند (مثل ساعت ها یا سمعک ها).
باتری های قلیایی
باتریهای قلیایی به عنوان یکی دیگر از انواع باتری به شمار می روند که غیرقابل شارژ هستند. این نوع از باتری ها در اسباب بازیها، قطعات الکترونیکی و ضبط صوتهای همراه کاربرد دارند. به دلیل سرعت پایین از دست دادن خودبخودی شارژ و نداشتن فلزات سنگین سمی، باتری های محبوبی هستند. در این باتری ها، فلز روی به عنوان آند و منگنز دی اکسید به عنوان کاتد استفاده شده اند. نام آن ها نیز برگرفته از محلول قلیایی (معمولاً پتاسیم هیدروکسید) می باشد که نقش الکترولیت را دارد.
باتری های ثانویه
این نوع از باتریها با نام سلول های ثانویه نیز شناخته می شوند. پس از استفاده از این باتری ها، می توان آنها را با عبور جریان از میان الکترودها در جهت مخالف، شارژ نمود. منظور از جهت مخالف این است که از قطب منفی به قطب مثبت، شارژ شوند.
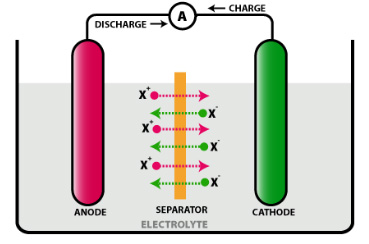
باتری های ثانویه از سلول های الکتروشیمیایی استفاده می کنند که واکنش های شیمیایی در آنها با اعمال ولتاژی خاص به باتری، معکوس می شود. به عبارت دیگر در هنگام شارژ، الکترون ها از سمت کاتد به سمت آند حرکت می کنند. اما، در هنگام استفاده و تخلیه شارژ (دِشارژ) حرکت الکترون ها از سمت آند به سمت کاتد است. به دلیل اینکه این باتری ها را پس از کاهش شارژ آنها می توان مجدد شارژ کرد، به آنها باتری قابل شارژ گفته می شود. از این باتری ها به عنوان اینورتر برای تأمین انرژی استفاده می شود.
برخی از باتری های مهم و رایج قابل شارژ که در صنعت مورد استفاده قرار می گیرند، عبارتند از:
- باتری های سربی – اسیدی
- باتری های نیکل – کادمیم (Ni-Cd)
- باتری های نیکل – هیبرید فلز
- باتری های یون لیتیم (Li-ion)
- باتری های قلیایی
- باتری های سربی – اسیدی
باتری های سربی- اسیدی
در اواخر سال های 1850 توسعه یافتند. اساس کار این باتری ها کوپل الکتروشیمیایی سرب- دی اکسید سرب است. الکترولیت مورد استفاده در این نوع باتری ها نیز سولفوریک اسید می باشد. این اسید باعث شده این باتری ها بسیار ارزان بوده و در بیشتر خودروها و وسایل نقلیه برای تأمین نیروی سیستم روشنایی استفاده شوند. اساس کار این باتری ها سرب درون آن هاست. در واقع، هر دو الکترود (یا همان رساناهایی که الکتریسیته از طریق آنها وارد باتری شده یا از آن خارج می شود)، حاوی مقداری سرب هستند. آند از سرب فلزی و کاتد از دی اکسید سرب ساخته شده اند. الکترودها درون محلول الکترولیتی از جنس سولفوریک اسید که حاوی یون های هیدروژن و یون های بی سولفات است، قرار دارند.
سرب قرار گرفته در قسمت آند از طریق الکترولیت با بی سولفات واکنش داده، الکترون های آزاد و سولفات سرب تولید می کند. الکترون ها به سمت کاتد رفته، با دی اکسید سربِ کاتد واکنش می دهند. این واکنش نیز سولفات سرب تولید می کند، که باعث می شود فرآیند بالا مجدد تکرار شود.

باتری های سربی- اسیدی نسبت به باتری های قابل شارژ امروزی، دانسیته انرژی نسبتاً کمی دارند. ظرفیت این باتری ها 2 تا 24 ولت بوده و معمولاً در ظرفیت های 2، 6، 12 و 24 ولت وجود دارند. از انجایی که این باتری ها قیمت کمی دارند، فراهم کردن جریان بالای مورد نیاز موتورهای استارتر باعث شده تا برای استفاده در وسایل نقلیه موتوری گزینه مطلوبی باشند.
در واقع، این باتری ها دارای اندازه های بزرگی هستند که در تجهیزات مختلف صنعتی از جمله لیفتراک های صنعتی کاربرد دارند. باتری های سربی- اسیدی نسبت به سایر باتری های صنعتی اندازه بزرگتر داشته ولی قیمت آن ها پایین تر است. به همین دلیل برای صاحبان مشاغل که به دنبال کاهش هزینه هستند، گزینه مناسبی به نظر می رسند. باتری خودرو یک نمونه از این باتریهاست که از صفحات نازک سرب و اکسید سرب، تشکیل شده است.
باتری های نیکل – کادمیم
این باتری ها نوع دیگری از باتری های قابل شارژ است که از اکسید هیدروکسید نیکل و کادمیم فلزی به عنوان الکترود استفاده می کند. در واقع اکسی هیدروکسید نیکل به عنوان الکترود مثبت و فلز کادمیم الکترود منفی را تشکیل می دهند. محلولی از پتاسیم هیدروکسید نیز به عنوان الکترولیت استفاده شده است. یکی از مزایای این باتری ها این است که آنها قابلیت نگهداری ولتاژ و بار را در هنگامی که از آنها استفاده نمی شوند، دارند. این باتری ها قیمت کمی داشته و نسبت به باتری های نیکل هیدروکسید فلز نرخ تخلیه بسیار کمتری دارند.
این نوع باتری ها در اندازه ها و ظرفیت های مختلفی وجود دارند. اندازه های کوچک آنها در اسباب بازی ها، ابزارهای الکترونیکی و دستگاه های پورتابل کاربرد دارند. از اندازه بزرگتر آنها نیز در باتری های روشن کننده هواپیما و وسایل الکتریکی استفاده می شود.
مشکل این باتری ها این است که مستعد اثر حافظه هستند. این بدین معنی است که باتری دشارژهای قبلی را به خاطر آورده و بنابراین شارژمجدد آن به درستی انجام نخواهد شد. برای همین اطمینان از دشارژ یا تخلیه شارژ صحیح قبل از شارژ مجدد این باتری ها امری ضروری است. مشکل دیگر نیز این است که کادمیم فلزی گران و سمی است که باعث آسیب به محیط زیست می شود.
باتری های نیکل کادمیم محبوبیت بالایی دارند که به دلیل کارایی و عملکرد بالای آن هاست. البته نگهداری و مراقبت از این باتری ها نسبت به سایر بانتری های صنعتی هزینه بیشتری در بردارد. علاوه بر این، هزینه اولیه تهیه این باتری ها نیز حدوداً 4 برابر باتری های سرب اسیدی است.
باتری های نیکل- هیبرید فلز (Ni-MH)
باتری های نیکل –هیبرید فلز باتری های قابل شارژی هستند که در ابزارهای الکترونیکی مانند گوشی های هوشمند، لپ تاپ ها، کامپیوترها و … کاربرد دارند. مشکلات مربوط به باتری های نیکل کادمیم موجب شد تا آند کادمیم با یک آلیاژ بین فلزی جاذب هیدروژن جایگزین شود. اما، واکنش شیمیایی در الکترود مثبت شبیه به واکنشی است که درسلول نیکل- کادمیم با استفاده از هم اکسید و هم هیدروکسید نیکل می بینیم.
الکترود ترکیبی از یک فلز نادر خاکی مانند لانتالم، سریم یا نئودیم به همراه نیکل، کبالت، منگنز یا آلومینیوم است. الکترون های تأمین کننده جریان مدار، حاصل اکسیداسیون اتم های هیدروژن هستند که تبدیل به پروتون می شوند. این پروتون ها با یون های هیدروکسید حاصل از الکترولیت واکنش می دهند و آب تولید می شود. آلیاژ فلزی تشکیل دهنده آند در واکنش شرکت نمی کند و فقط محیطی برای یون های مهم هیدریدی است. این باتری ها به لحاظ ولتاژ، ظریفت و کاربرد بسیار شبیه باتری های نیکل کادمیم هستند.

باتری های یون لیتیم
این نوع باتری ها متشکل از سلول هایی هستند که در آن ها در حین دِشارژ یون های لیتیم از الکترود منفی به سمت الکترود مثبت حرکت می کنند. این حرکت در حین شارژ برعکس می شود. در واقع، باتری های یون لیتیم انرژی را از طریق ایجاد اختلاف پتانسیل بین قطب های مثبت و منفی باتری ذخیره می کنند. یک لایه عایق به نام جداکننده دو طرف باتری را از هم جدا کرده و جلوی حرکت الکترون ها را سد می کند. حرکت یون های لیتیم، موجب ایجاد اختلاف پتانسیل ذکر شده می شود. این اختلاف پتانسیل «ولتاژ» نامیده می شود.
هنگامی که شما دستگاه الکترونیکی خود را به باتری لیتیم متصل می کنید شارژ آغاز می گردد. الکترون هایی که توسط جداکننده این باتری ها قفل شده بودند، از جداکننده عبور کرده و دستگاه را شارژ می کنند. باتری های یون لیتیم دارای انواع مختلفی بوده و بسیار پرکاربرد هستند. امروزه در انواع لپ تاپ ها، گوشی های هوشمند، دوربین ها و غیره از این نوع باتری ها استفاده می شود. این نوع از باتریها معمولاً نسبت به سایر باتری ها دارای دانسیته انرژی بالاتر، اثر حافظه کم یا عدم اثر حافظه، و تخلیه خودبخودی شارژ کمتری هستند.

باتری های یون لیتیم به دلیل داشتن وزن کم بهترین گزینه برای استفاده در صنایع می باشند. به دلیل داشتن چگالی بالا در موارد مختلفی مثل گوشی موبایل، هواپیماها سایر موارد از این باتری ها استفاده می شود. باتری های یون لیتیم به دلیل سبکی برای تأمین انرژی لیفتراک های صنعتی گزینه مطلوبی به شمار می روند. زیرا علاوه بر اینکه سبک هستند، با شارژ شدن سریع می توانند افزایش عملکرد لیفتراک را در پی داشته باشند. هزینه اولیه مربوط به تهیه باتری های یون لیتیم تقریباً 2 برابر هزینه ای است که برای باتری های سرب اسیدی می شود. البته ناگفته نماند که این قیمت بالا، با عمر طولانی و کوتاه بودن زمان شارژ جبران می شود.


